14/01/2026
En el vasto y dinámico universo de la química, donde miles de millones de reacciones ocurren constantemente a nuestro alrededor y dentro de nosotros, existe un concepto fundamental que actúa como el guardián de estas transformaciones: la energía libre de activación. No es simplemente una medida; es el peaje energético que las moléculas deben pagar para iniciar su viaje hacia nuevos estados, el trampolín invisible que determina la velocidad y la viabilidad de cualquier proceso químico. Comprender qué es la energía libre de activación, simbolizada como ΔG≠, nos permite desentrañar los misterios de por qué algunas reacciones son instantáneas y otras requieren un empujón considerable, abriendo la puerta a la manipulación y el control de la materia a nivel molecular.

La energía libre de activación (ΔG≠) es, en esencia, la cantidad mínima de energía que se requiere para que un mol de una sustancia, a una temperatura dada, alcance el estado de transición. Este estado de transición es un punto de no retorno en la trayectoria de una reacción, la cima de una barrera energética donde los enlaces antiguos se están rompiendo y los nuevos se están formando simultáneamente. No es un intermediario estable, sino una configuración molecular fugaz y de muy alta energía, inestable y efímera, que representa el punto de máxima energía potencial en el camino de los reactivos a los productos. Es el paso más lento y limitante de la velocidad de una reacción, y su magnitud es un factor determinante en la velocidad a la que una reacción puede ocurrir. Una ΔG≠ alta implica una reacción lenta, mientras que una ΔG≠ baja sugiere una reacción rápida, ya que un mayor número de moléculas poseerá la energía cinética suficiente para superar esta barrera.
- La Naturaleza de la Barrera Energética
- Factores que Influyen en la Velocidad de Reacción a Través de ΔG≠
- Importancia de la Energía Libre de Activación en Diversos Campos
- Distinción de Otros Conceptos Energéticos
- Representación Gráfica: Diagramas de Coordenadas de Reacción
- Preguntas Frecuentes sobre la Energía Libre de Activación
La Naturaleza de la Barrera Energética
Para que los reactivos se conviertan en productos, las moléculas deben chocar con la orientación correcta y con suficiente energía. No todas las colisiones son productivas; solo aquellas que superan la barrera de energía libre de activación resultan en una transformación química. Esta barrera se debe a la necesidad de superar las repulsiones intermoleculares, romper enlaces existentes y reordenar los átomos antes de que se puedan formar nuevos enlaces. La ΔG≠ incorpora no solo la energía (entalpía) necesaria para alcanzar el estado de transición, sino también los cambios en el desorden o la aleatoriedad (entropía) que ocurren durante la formación de este estado inestable. Es por eso que se utiliza el término 'energía libre' de activación, reflejando su dependencia de la temperatura y su relación con la energía de Gibbs, una medida termodinámica que predice la espontaneidad de un proceso.
Componentes de la Energía Libre de Activación
- Entalpía de Activación (ΔH≠): Representa la energía térmica necesaria para romper los enlaces iniciales y formar los nuevos en el estado de transición. Es la parte 'energética' de la barrera.
- Entropía de Activación (ΔS≠): Refleja el cambio en el desorden o la organización del sistema cuando los reactivos se transforman en el estado de transición. Una disminución en la entropía de activación (ΔS≠ negativa) indica que el estado de transición es más ordenado que los reactivos, lo que añade una penalización energética a la ΔG≠.
La relación que los une es similar a la de la energía libre de Gibbs global de una reacción: ΔG≠ = ΔH≠ - TΔS≠. Esta ecuación subraya la complejidad de la barrera energética, mostrando que no solo la energía necesaria es importante, sino también cómo se organizan las moléculas en ese punto crítico.
Factores que Influyen en la Velocidad de Reacción a Través de ΔG≠
Aunque la energía libre de activación es una característica intrínseca de una reacción dada, su impacto en la velocidad de la reacción puede ser modulado por diversos factores externos. Sin embargo, es crucial entender que estos factores no cambian el valor de ΔG≠ en sí misma (que es una propiedad termodinámica de la reacción), sino que alteran la proporción de moléculas que pueden superar esa barrera.
1. Temperatura
Un aumento en la temperatura incrementa la energía cinética promedio de las moléculas. Esto significa que una mayor fracción de moléculas tendrá suficiente energía para alcanzar o superar la energía libre de activación, lo que resulta en un aumento significativo de la velocidad de reacción. La relación es exponencial: un pequeño aumento de temperatura puede duplicar o triplicar la velocidad de una reacción.
2. Concentración de Reactivos
Aunque la concentración no afecta directamente la ΔG≠, un aumento en la concentración de los reactivos incrementa la frecuencia de las colisiones moleculares. Más colisiones significan más oportunidades para que las moléculas con la energía y orientación correctas superen la barrera de activación, llevando a una mayor velocidad de reacción.
3. Catalizadores
Los catalizadores son sustancias extraordinarias que tienen la capacidad de acelerar drásticamente la velocidad de una reacción sin ser consumidos en el proceso. Lo logran proporcionando un camino de reacción alternativo, un mecanismo diferente con una energía libre de activación significativamente menor (una ΔG≠ más baja). Esto permite que una mayor proporción de moléculas supere la barrera energética a la misma temperatura, aumentando la velocidad de reacción. Los catalizadores son ubicuos en la naturaleza (por ejemplo, las enzimas biológicas) y en la industria.
Importancia de la Energía Libre de Activación en Diversos Campos
El concepto de energía libre de activación trasciende las aulas de química y se manifiesta como un principio fundamental en una miríada de disciplinas, desde los procesos biológicos que sustentan la vida hasta las complejas ingenierías industriales.
En Biología y Bioquímica
La vida misma es una danza controlada de reacciones químicas, y la energía libre de activación es el director de orquesta. Las enzimas, que son catalizadores biológicos (generalmente proteínas), son maestras en la reducción de la ΔG≠. Sin enzimas, muchas reacciones metabólicas esenciales, como la digestión de alimentos o la síntesis de ADN, ocurrirían a velocidades tan lentas que la vida tal como la conocemos sería imposible. Las enzimas actúan uniendo los sustratos en una conformación específica que favorece la formación del estado de transición, disminuyendo así la energía necesaria para que la reacción proceda.
En la Industria Química
En la fabricación de productos químicos, la eficiencia y la rentabilidad son primordiales. Comprender y manipular la energía libre de activación es crucial para diseñar procesos industriales. Los químicos buscan catalizadores que permitan que las reacciones ocurran a temperaturas y presiones más bajas, lo que no solo reduce los costos energéticos, sino que también mejora la seguridad y la selectividad de los productos. Ejemplos incluyen la producción de amoníaco (proceso Haber-Bosch), la refinación de petróleo y la síntesis de polímeros.
En Ciencia de Materiales
La degradación de materiales, la corrosión, la polimerización y la durabilidad de los productos están intrínsecamente ligadas a la energía libre de activación de las reacciones subyacentes. Entender la ΔG≠ permite a los científicos diseñar materiales más resistentes, predecir su vida útil y desarrollar métodos para ralentizar o acelerar procesos de cambio de fase.
Distinción de Otros Conceptos Energéticos
Es común confundir la energía libre de activación con otros conceptos energéticos en termodinámica y cinética química. Es vital diferenciarlos para una comprensión clara:
| Concepto | Símbolo | Descripción | Rol en la Reacción |
|---|---|---|---|
| Energía Libre de Activación | ΔG≠ | Energía necesaria para alcanzar el estado de transición. | Determina la velocidad de reacción. |
| Energía Libre de Gibbs | ΔG | Cambio total de energía libre entre productos y reactivos. | Determina la espontaneidad (si la reacción ocurre o no). |
| Cambio de Entalpía | ΔH | Cambio de calor total entre productos y reactivos. | Determina si una reacción es exotérmica o endotérmica. |
| Energía de Activación (Arrhenius) | Ea | Parámetro empírico derivado de la ecuación de Arrhenius. | Relacionado con ΔG≠, pero a menudo se asume que incluye solo el componente entálpico. |
Mientras que ΔG (la energía libre de Gibbs global de la reacción) nos dice si una reacción es espontánea o no, no nos dice nada sobre su velocidad. Una reacción puede ser termodinámicamente favorable (ΔG negativa) pero cinéticamente lenta (ΔG≠ alta). Por ejemplo, el diamante es termodinámicamente inestable y debería convertirse en grafito, pero la ΔG≠ para esta transformación es tan alta que el proceso es imperceptible en la escala de tiempo humana.
Representación Gráfica: Diagramas de Coordenadas de Reacción
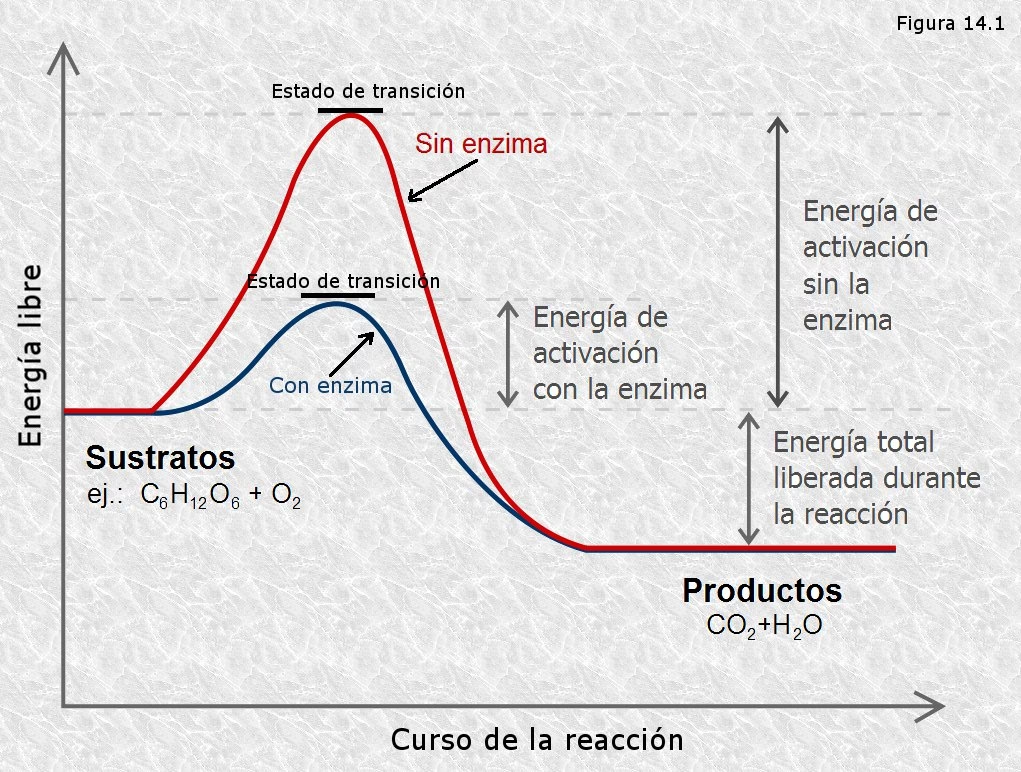
La energía libre de activación se visualiza mejor a través de un diagrama de coordenadas de reacción. En este gráfico, el eje Y representa la energía potencial (o energía libre) y el eje X representa la 'coordenada de reacción', que es una medida del progreso de la reacción desde los reactivos hasta los productos. La barrera energética de activación se muestra como una 'joroba' o 'pico' en el perfil de energía. La cima de esta joroba es el estado de transición, y la altura de la joroba desde la energía de los reactivos hasta la cima es la energía libre de activación (ΔG≠). Un diagrama de este tipo también ilustra el cambio de energía libre global (ΔG) como la diferencia entre la energía de los reactivos y la energía de los productos.
Preguntas Frecuentes sobre la Energía Libre de Activación
¿Es la energía de activación siempre positiva?
Sí, la energía libre de activación (ΔG≠) es casi siempre positiva. Esto significa que el estado de transición es, por definición, un estado de mayor energía que los reactivos. Si fuera negativa, la reacción ocurriría instantáneamente sin una barrera energética significativa, lo cual es extremadamente raro en reacciones químicas ordinarias. En casos muy específicos, como reacciones radicalarias o de recombinación, puede ser cercana a cero, pero nunca negativa en el sentido de una barrera.
¿Puede una reacción ocurrir sin energía de activación?
Teóricamente, no. Toda reacción requiere de alguna energía para reorganizar los enlaces. Sin embargo, algunas reacciones tienen una energía de activación tan baja que ocurren a velocidades extremadamente rápidas incluso a temperatura ambiente, casi pareciendo instantáneas. Esto es común en reacciones iónicas o aquellas con una alta fuerza impulsora termodinámica.
¿Cómo actúan los catalizadores para reducir la energía de activación?
Los catalizadores no alteran la energía de los reactivos ni de los productos, ni la espontaneidad global de la reacción (ΔG). En su lugar, proporcionan un mecanismo o ruta de reacción alternativa que tiene un estado de transición de menor energía. Esto se logra estabilizando el estado de transición, orientando las moléculas reactivas de manera más favorable, o facilitando la ruptura de enlaces, reduciendo así la energía necesaria para alcanzar el punto crítico de la reacción.
¿Cuál es la diferencia entre energía de activación y estado de transición?
La energía de activación (ΔG≠) es la *cantidad de energía* necesaria para alcanzar el estado de transición. El estado de transición es la *estructura molecular o configuración* de máxima energía a lo largo de la coordenada de reacción, un punto intermedio inestable y fugaz entre los reactivos y los productos. Es el pico de la barrera energética, mientras que la energía de activación es la altura de ese pico desde la base de los reactivos.
¿Por qué se le llama 'energía libre' de activación?
Se le llama 'energía libre' porque, al igual que la energía libre de Gibbs (ΔG) de la reacción global, considera no solo el componente de entalpía (energía térmica) sino también el componente de entropía (desorden) asociado con la formación del estado de transición. La ecuación ΔG≠ = ΔH≠ - TΔS≠ muestra que la energía necesaria para alcanzar el estado de transición depende tanto de la energía de los enlaces como de cómo se organizan las moléculas en ese punto crítico y de la temperatura del sistema.
En resumen, la energía libre de activación es un concepto central en la cinética química que explica por qué las reacciones ocurren a ciertas velocidades. Es la clave para entender y controlar las transformaciones químicas, desde las más simples hasta las más complejas, y su manipulación a través de catalizadores ha revolucionado la industria y nuestra comprensión de la vida misma.
Si quieres conocer otros artículos parecidos a Energía Libre de Activación: El Umbral Vital de las Reacciones Químicas puedes visitar la categoría Librerías.