27/09/2024
La tabla periódica de los elementos no es solo un póster en las aulas de ciencia; es la Rosetta Stone de la química, una herramienta indispensable que organiza y revela los secretos de toda la materia que nos rodea. Desde el aire que respiramos hasta los metales más pesados, cada sustancia fundamental tiene su lugar y sus propiedades definidas en este ingenioso mapa. Comprenderla es abrir una ventana a la composición del universo y al comportamiento de los elementos.
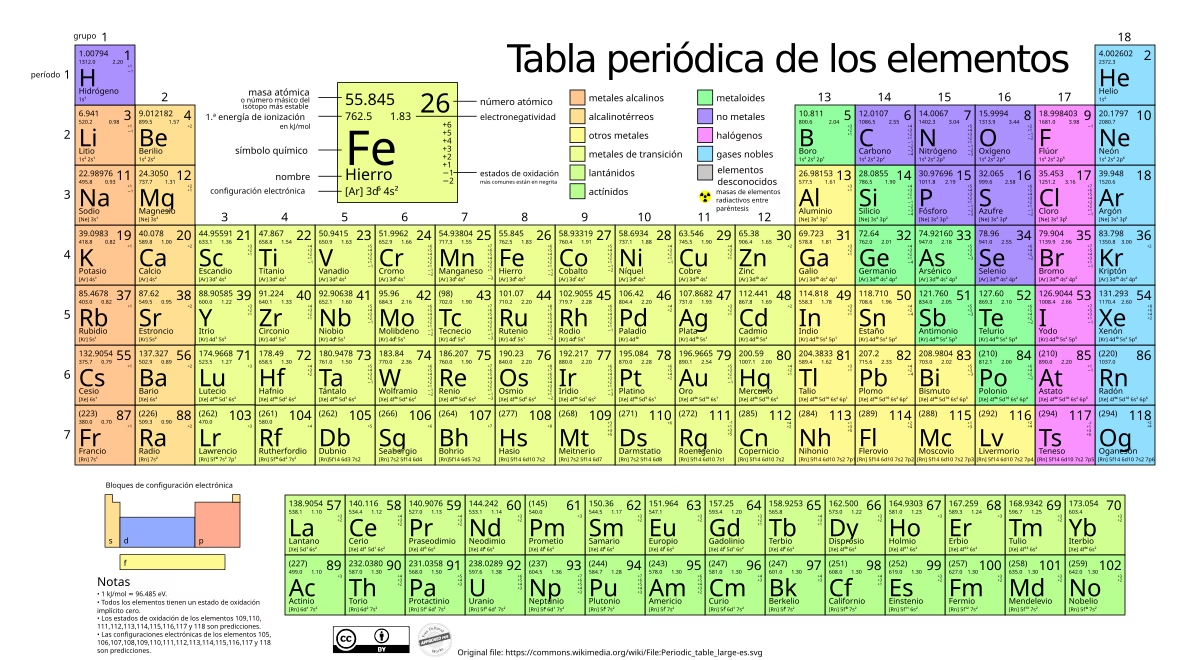
En este artículo, desglosaremos la tabla periódica, explorando su estructura, su historia y su inmensa relevancia en el mundo moderno. Aprenderás a interpretar la información que cada elemento nos ofrece y descubrirás por qué esta organización es una de las mayores proezas intelectuales de la ciencia.
- Decodificando el Lenguaje de los Elementos: Cómo Leer la Tabla Periódica
- Un Viaje en el Tiempo: La Fascinante Historia de la Tabla Periódica
- Más Allá de la Química: ¿Por Qué la Tabla Periódica es Indispensable?
- Estructura Maestra: Periodos, Grupos y Bloques
- Visión General: Tabla de Periodos y Elementos
- Preguntas Frecuentes sobre la Tabla Periódica
Decodificando el Lenguaje de los Elementos: Cómo Leer la Tabla Periódica
Cada pequeño recuadro en la tabla periódica es una ficha de identidad para un elemento, repleta de información crucial. Aunque el diseño puede variar ligeramente, la mayoría de las entradas de elementos comparten características comunes:
- Símbolo Químico: Es la abreviatura universal del elemento. Generalmente consta de una o dos letras, la primera siempre en mayúscula. Por ejemplo, “O” para oxígeno, “C” para carbono, y “Na” para sodio (derivado de su nombre en latín, natrium). Estos símbolos facilitan la comunicación global entre científicos, trascendiendo las barreras del idioma.
- Número Atómico (Z): Ubicado típicamente en la parte superior del recuadro, es el número de protones en el núcleo del átomo del elemento. Este número es la 'identidad' única de un elemento; si cambia el número atómico, cambia el elemento. Por ejemplo, el Carbono siempre tiene un número atómico de 6.
- Nombre del Elemento: El nombre completo del elemento, como 'Oxígeno' o 'Hierro'.
- Masa Atómica (Peso Atómico): Usualmente se encuentra debajo del nombre del elemento. Representa la masa promedio de los átomos de un elemento, considerando sus isótopos (átomos del mismo elemento con diferente número de neutrones). Se mide en unidades de masa atómica (uma).
Al entender estos componentes básicos, ya tienes la clave para empezar a desvelar la información que cada elemento te ofrece. La posición de un elemento en la tabla también es fundamental, ya que indica sus propiedades químicas y cómo interactuará con otros elementos.
Un Viaje en el Tiempo: La Fascinante Historia de la Tabla Periódica
La historia de la tabla periódica es un testimonio del ingenio humano y la búsqueda de orden en la naturaleza. Antes de su creación, los científicos luchaban por clasificar los elementos de manera coherente. Fue el químico ruso Dimitri Mendeléiev quien, en 1869, logró desarrollar un sistema de organización verdaderamente efectivo.
Mendeléiev ordenó los elementos conocidos en filas y columnas basándose en sus propiedades químicas y su peso atómico creciente. Lo revolucionario de su enfoque fue que, si un elemento no encajaba perfectamente en una posición, dejaba un espacio en blanco. Esta audaz decisión le permitió prever la existencia y las propiedades de elementos aún no descubiertos, como el galio y el germanio, que fueron encontrados años después con propiedades casi idénticas a las predichas. Su visión transformó la química de una ciencia descriptiva a una predictiva.
Con el tiempo, la tabla periódica evolucionó. A principios del siglo XX, Henry Moseley demostró que el orden de los elementos debía basarse en su número atómico (el número de protones), no en su peso atómico. Esta corrección resolvió algunas anomalías en la tabla de Mendeléiev y solidificó su estructura. Desde entonces, la tabla ha crecido hasta incluir 118 elementos, desde el ligero hidrógeno hasta el pesado oganesón, con los elementos más pesados siendo sintetizados en laboratorios.
Más Allá de la Química: ¿Por Qué la Tabla Periódica es Indispensable?
La tabla periódica es mucho más que una simple lista de elementos; es una herramienta esencial que impulsa el avance científico y tecnológico en innumerables campos. Su importancia radica en varias funciones clave:
- Organización y Clasificación Sistemática: Permite organizar los elementos de manera lógica, revelando patrones y tendencias en sus propiedades. Esto facilita su estudio y comprensión, haciendo que la química sea más accesible y sistemática.
- Predicción de Propiedades: Gracias a su estructura, los químicos pueden predecir con gran precisión las propiedades de elementos aún no descubiertos o sintetizados. Esta capacidad predictiva es fundamental para el diseño de nuevos materiales y compuestos. Por ejemplo, si un nuevo elemento se sintetiza y se coloca en el grupo de los halógenos, se esperaría que sea muy reactivo, formando sales con metales alcalinos.
- Símbolos y Nomenclatura Estándar: Al utilizar símbolos y nombres universales, la tabla periódica facilita la comunicación entre científicos de todo el mundo, eliminando ambigüedades y confusiones en la identificación de los elementos y sus compuestos. Es un lenguaje común para la ciencia.
- Aplicaciones Prácticas y Tecnológicas: El conocimiento de los elementos y sus propiedades es la base de innumerables aplicaciones. En medicina, ayuda en el desarrollo de fármacos y técnicas de diagnóstico. En la industria, es crucial para la creación de nuevos materiales (aleaciones, polímeros), catalizadores y procesos de fabricación. En energía, es fundamental para el diseño de baterías, paneles solares y reactores nucleares. En tecnología, permite el desarrollo de semiconductores, pantallas y dispositivos electrónicos cada vez más avanzados.
En esencia, la tabla periódica es la base sobre la que se construye gran parte de la ciencia y la tecnología modernas, permitiéndonos manipular la materia y crear innovaciones que transforman nuestras vidas.
Estructura Maestra: Periodos, Grupos y Bloques
La belleza de la tabla periódica reside en su estructura bidimensional, que organiza los elementos no solo por su número atómico sino también por sus propiedades periódicas, que se repiten con regularidad.
Los Periodos: Horizontes de Energía
La tabla periódica se divide en siete periodos, que corresponden a las siete filas horizontales de elementos. Cada periodo se distingue por el nivel de energía principal (o capa electrónica) que ocupan los electrones de valencia de los átomos de los elementos. A medida que te mueves de izquierda a derecha en un periodo, el número atómico aumenta en una unidad, y los electrones se añaden a la misma capa de valencia.
El periodo más corto de la tabla periódica es el Periodo 1, que contiene solamente dos elementos: el hidrógeno (H) y el helio (He). Esto se debe a que la primera capa electrónica solo puede albergar un máximo de dos electrones. A continuación, se detallan los nombres y elementos de cada periodo:
- Periodo 1: Hidrógeno (H), Helio (He).
- Periodo 2: Litio (Li), Berilio (Be), Boro (B), Carbono (C), Nitrógeno (N), Oxígeno (O), Flúor (F), Neón (Ne).
- Periodo 3: Sodio (Na), Magnesio (Mg), Aluminio (Al), Silicio (Si), Fósforo (P), Azufre (S), Cloro (Cl), Argón (Ar).
- Periodo 4: Potasio (K), Calcio (Ca), Escandio (Sc), Titanio (Ti), Vanadio (V), Cromo (Cr), Manganeso (Mn), Hierro (Fe), Cobalto (Co), Níquel (Ni), Cobre (Cu), Zinc (Zn), Galio (Ga), Germanio (Ge), Arsénico (As), Selenio (Se), Bromo (Br), Kriptón (Kr).
- Periodo 5: Rubidio (Rb), Estroncio (Sr), Itrio (Y), Circonio (Zr), Niobio (Nb), Molibdeno (Mo), Tecnecio (Tc), Rutenio (Ru), Rodio (Rh), Paladio (Pd), Plata (Ag), Cadmio (Cd), Indio (In), Estaño (Sn), Antimonio (Sb), Telurio (Te), Yodo (I), Xenón (Xe).
- Periodo 6: Cesio (Cs), Bario (Ba), y los elementos de las series de los Lantánidos (del Lantano al Lutecio, 15 elementos), Hafnio (Hf), Tántalo (Ta), Tungsteno (W), Renio (Re), Osmio (Os), Iridio (Ir), Platino (Pt), Oro (Au), Mercurio (Hg), Talio (Tl), Plomo (Pb), Bismuto (Bi), Polonio (Po), Astato (At), Radón (Rn).
- Periodo 7: Francio (Fr), Radio (Ra), y los elementos de las series de los Actínidos (del Actinio al Lawrencio, 15 elementos), Rutherfordio (Rf), Dubnio (Db), Seaborgio (Sg), Bohrio (Bh), Hassio (Hs), Meitnerio (Mt), Darmstadtio (Ds), Roentgenio (Rg), Copernicio (Cn), Nihonio (Nh), Flerovio (Fl), Moscovio (Mc), Livermorio (Lv), Tennesso (Ts), Oganesón (Og).
Los Grupos: Familias con Propiedades Similares
Las columnas verticales de la tabla periódica se denominan grupos o familias. Los elementos dentro de un mismo grupo comparten un número similar de electrones en su capa más externa (electrones de valencia), lo que les confiere propiedades químicas muy parecidas. Por ejemplo:
- Grupo 1 (Metales Alcalinos): Son metales muy reactivos que tienden a perder un electrón para formar iones con carga +1.
- Grupo 17 (Halógenos): Son no metales muy reactivos que tienden a ganar un electrón para formar iones con carga -1.
- Grupo 18 (Gases Nobles): Son elementos muy estables y poco reactivos, ya que tienen su capa de valencia completa.
Existen 18 grupos en la tabla periódica, cada uno con sus propias características distintivas, que son fundamentales para entender cómo reaccionan los elementos.

Los Bloques: s, p, d, y f
Más allá de los periodos y grupos, la tabla periódica también se puede dividir en cuatro bloques principales: s, p, d y f. Estos bloques corresponden a los subniveles de energía donde se encuentran los electrones de valencia de los elementos. Esta clasificación ayuda a comprender las configuraciones electrónicas y, por ende, las propiedades de los elementos.
- Bloque s: Incluye los Grupos 1 y 2 (Metales Alcalinos y Alcalinotérreos).
- Bloque p: Abarca los Grupos 13 al 18.
- Bloque d: Comprende los Grupos 3 al 12 (Metales de Transición).
- Bloque f: Corresponde a las series de los Lantánidos y Actínidos, usualmente ubicadas debajo de la tabla principal para mantener su formato compacto.
Visión General: Tabla de Periodos y Elementos
Para una referencia rápida, aquí se muestra un resumen de los periodos y el número de elementos que contiene cada uno:
| Periodo | Número de elementos |
|---|---|
| 1 | 2 |
| 2 | 8 |
| 3 | 8 |
| 4 | 18 |
| 5 | 18 |
| 6 | 32 |
| 7 | 32 |
Preguntas Frecuentes sobre la Tabla Periódica
A continuación, respondemos algunas de las preguntas más comunes sobre esta herramienta fundamental de la química:
¿Cuántos elementos hay en la tabla periódica?
Actualmente, la tabla periódica cuenta con 118 elementos conocidos, desde el hidrógeno (H) hasta el oganesón (Og).
¿Cuál es el elemento más ligero de la tabla periódica?
El hidrógeno (H) es el elemento más ligero de la tabla periódica, con un número atómico de 1.
¿Cuál es el periodo más largo de la tabla periódica?
Los periodos 6 y 7 son los más largos de la tabla periódica, cada uno conteniendo 32 elementos. Esto incluye las series de lantánidos y actínidos, que se muestran aparte para mantener la legibilidad de la tabla.
¿Cuál es el periodo más corto de la tabla periódica?
El periodo 1 es el más corto de la tabla periódica, ya que solo contiene 2 elementos: hidrógeno y helio.
¿Qué representa el número atómico?
El número atómico (Z) representa la cantidad de protones en el núcleo de un átomo. Es la característica que define a un elemento químico.
¿Qué es la masa atómica?
La masa atómica es la masa promedio de los átomos de un elemento, considerando la abundancia de sus isótopos naturales. Se expresa en unidades de masa atómica (uma).
La tabla periódica de los elementos es, sin duda, una de las herramientas más poderosas y elegantes en el estudio de la química y las ciencias en general. Su capacidad para organizar, clasificar y predecir el comportamiento de los elementos la convierte en una pieza clave para cualquier científico o entusiasta del conocimiento. Con cada nuevo descubrimiento o síntesis de un elemento, la tabla periódica se actualiza, demostrando ser un documento vivo y en constante evolución, reflejo de nuestra creciente comprensión del universo.
Si quieres conocer otros artículos parecidos a Desvelando los Secretos de la Tabla Periódica puedes visitar la categoría Librerías.
