30/06/2022
El ácido láctico, un compuesto cuyo nombre evoca directamente su origen en la leche (del latín lac, lactis), es mucho más que un simple subproducto lácteo. Es una molécula fundamental con roles protagónicos en la bioquímica, desde la vital fermentación láctica hasta su presencia en nuestros propios músculos. Su versatilidad química y biológica lo convierte en un sujeto de estudio constante, no solo por su importancia intrínseca sino también por la posibilidad de derivar de él compuestos con aplicaciones específicas, como el nitrilo del ácido láctico.
Este artículo explorará en profundidad qué es el ácido láctico, su estructura, sus isómeros y su trascendencia biológica. Pero, sobre todo, nos sumergiremos en el fascinante proceso de cómo se forma el nitrilo de este ácido en un entorno de laboratorio, desentrañando la química detrás de esta síntesis. Además, abordaremos sus diversas aplicaciones y desmentiremos algunos mitos comunes asociados a él, ofreciendo una visión completa de este compuesto tan singular.
- El Ácido Láctico: Un Compuesto Versátil
- ¿Cómo se Forma el Nitrilo del Ácido Láctico? La Síntesis de Laboratorio
- La Producción Biológica del Ácido L-Láctico
- Desmintiendo Mitos: Ácido Láctico, Ejercicio y Dolor Muscular
- Aplicaciones Sorprendentes del Ácido Láctico
- Preguntas Frecuentes sobre el Ácido Láctico y su Nitrilo
- ¿Qué diferencia hay entre el ácido láctico y el lactato?
- ¿Es el ácido láctico el causante de las agujetas o el dolor muscular?
- Si el lactato no causa acidosis, ¿qué la provoca durante el ejercicio intenso?
- ¿Cómo se produce el L-lactato en el cuerpo?
- ¿Cuál es la función del ciclo de Cori?
- ¿Se utiliza el ácido láctico en cosméticos? ¿Es seguro?
- ¿Se puede encontrar ácido láctico en alimentos que no sean lácteos?
El Ácido Láctico: Un Compuesto Versátil
El ácido láctico, sistemáticamente conocido como ácido 2-hidroxi-propanoico según la nomenclatura IUPAC, es un ácido carboxílico de fórmula H3C-CH(OH)-COOH. Su estructura es particular: posee un grupo hidroxilo (-OH) en el carbono adyacente al grupo carboxilo (-COOH), lo que lo clasifica como un ácido α-hidroxílico (AHA), una característica que le confiere propiedades únicas y lo hace de interés en diversas industrias, especialmente la cosmética. En soluciones acuosas y a pH fisiológico, este ácido puede perder un protón, transformándose en su forma disociada, el anión conocido como lactato.
Una de las propiedades más interesantes del ácido láctico es su quiralidad. Esto significa que posee un átomo de carbono asimétrico, lo que da lugar a dos isómeros ópticos o enantiómeros que son imágenes especulares no superponibles entre sí. Estos son el ácido D-(-)-láctico (también llamado ácido (R)-láctico) y el ácido L-(+)-láctico (o ácido (S)-láctico). La forma L-(+)-láctico es la que tiene mayor relevancia biológica y es la que nuestro cuerpo produce. Cuando ambos isómeros se encuentran en cantidades idénticas, se forma una mezcla racémica, conocida como d,l-ácido láctico.
Características Físicas y Químicas del Ácido Láctico
Para comprender mejor el ácido láctico, es útil conocer sus propiedades fundamentales:
| Característica | Valor |
|---|---|
| Fórmula Molecular | C3H6O2 |
| Fórmula Semidesarrollada | H3C-CH(OH)-COOH |
| Masa Molecular | 90.08 g/mol |
| Estado de Agregación (Condiciones Normales) | Líquido |
| Punto de Ebullición | 122 °C |
| Densidad Relativa | 1.206 g/cm3 |
| Acidez (pKa) | 3.5 |
| Solubilidad en Agua | Miscible (solubilidad alta) |
Estos datos nos dan una idea de su comportamiento en diferentes condiciones y su interacción con otras sustancias.
¿Cómo se Forma el Nitrilo del Ácido Láctico? La Síntesis de Laboratorio
La formación del nitrilo del ácido láctico es un proceso clave en la síntesis de laboratorio del propio ácido láctico racémico. Este método permite obtener el compuesto a partir de precursores más simples y es un ejemplo clásico de cómo la química orgánica puede construir moléculas complejas paso a paso. La reacción principal involucra el etanal (acetaldehído) y el cianuro de sodio, seguida de una etapa de saponificación.
El proceso se puede resumir en la siguiente ecuación global:
2CH3-COH + 2NaCN + 2H2SO4 + 4 H2O ==> 2CH3-CH(OH)-COOH + Na2SO4 + (NH4)2SO4
Analicemos los pasos de esta reacción:
- Ataque Nucleofílico del Cianuro al Etanal: La primera etapa de la formación del nitrilo es un ataque nucleofílico. El etanal (CH3-COH), que contiene un grupo carbonilo (C=O), es el electrófilo. El ion cianuro (CN-), proveniente del cianuro de sodio (NaCN), actúa como un nucleófilo fuerte. Este cianuro ataca el carbono del grupo carbonilo del etanal, que es deficiente en electrones debido a la polaridad del doble enlace C=O. Este ataque rompe el doble enlace y forma un nuevo enlace carbono-carbono, resultando en la adición del grupo cianuro al aldehído. Simultáneamente, el oxígeno del carbonilo se protona (generalmente por la presencia de agua o un ácido débil en el medio), formando un grupo hidroxilo. El producto intermedio de esta reacción es el 2-hidroxipropanonitrilo, que es el nitrilo del ácido láctico. Es importante destacar que esta adición nucleofílica al aldehído, al crear un nuevo centro quiral (el carbono con el grupo hidroxilo y el grupo ciano), produce el nitrilo del ácido láctico en una mezcla racémica, es decir, con cantidades iguales de sus dos enantiómeros (D y L).
- Saponificación del Nitrilo: Una vez formado el 2-hidroxipropanonitrilo, este se somete a una reacción de saponificación. La saponificación es una hidrólisis de un nitrilo en presencia de un ácido o una base fuerte. En este caso, el nitrilo se hidroliza en presencia de agua (H2O) y un exceso de ácido sulfúrico (H2SO4). Durante esta etapa, el grupo cianuro (-C≡N) se transforma en un grupo carboxilo (-COOH). Este proceso libera amoniaco (NH3) que reacciona con el ácido sulfúrico para formar sulfato de amonio ((NH4)2SO4). El resultado final de esta saponificación es la obtención del ácido láctico libre, también en su forma racémica, listo para ser aislado y purificado.
Esta síntesis en laboratorio es fundamental para la producción industrial de ácido láctico cuando no se recurre a la fermentación biológica, especialmente para aplicaciones donde una mezcla racémica es aceptable o incluso deseable.
La Producción Biológica del Ácido L-Láctico
Mientras que la síntesis de laboratorio produce una mezcla racémica, la naturaleza es mucho más específica. El ácido L-(+)-láctico, de vital importancia biológica, se produce de manera predominante en organismos vivos. Su formación es un proceso continuo dentro del metabolismo celular, especialmente relevante en tejidos con alta demanda energética como los músculos.
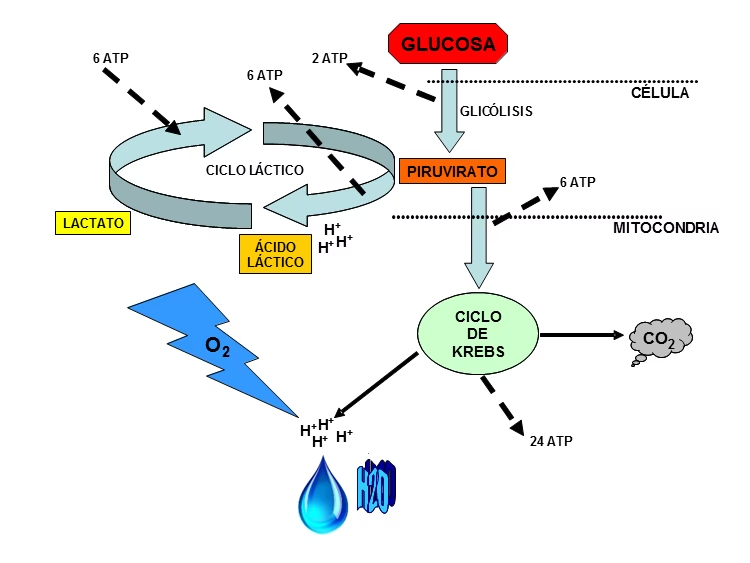
La ruta principal para la producción de L-lactato en el cuerpo humano es a partir del piruvato, una molécula clave en el metabolismo de los carbohidratos. Esta conversión es catalizada por una enzima crucial: la lactato deshidrogenasa (LDH). La reacción es la siguiente:
Piruvato + NADH + H+ → Lactato + NAD+
La función principal de esta reacción no es simplemente producir lactato, sino regenerar el dinucleótido de nicotinamida y adenina (NAD+) a partir de su forma reducida (NADH + H+). El NAD+ es un cofactor esencial para la glucólisis, el proceso metabólico que produce ATP (adenosín trifosfato), la principal moneda de energía de la célula. Al regenerar NAD+, la LDH asegura que la glucólisis pueda continuar, permitiendo una producción rápida de ATP incluso en condiciones de bajo oxígeno.
Durante el ejercicio intenso, la demanda de energía en los músculos supera la capacidad del metabolismo oxidativo (aeróbico) para producir ATP lo suficientemente rápido. En estas condiciones, la glucólisis se acelera y se convierte en la principal fuente de ATP. El piruvato se acumula rápidamente, y si no se convierte en lactato, inhibiría la glucólisis. La LDH interviene, convirtiendo el piruvato en lactato y, crucialmente, regenerando el NAD+ necesario para mantener la producción de energía. Es un mecanismo de supervivencia que permite al músculo seguir trabajando bajo esfuerzo.
El lactato producido en las células musculares no se queda allí; circula por el torrente sanguíneo hasta el hígado. En el hígado, el lactato puede ser reconvertido a piruvato y luego a glucosa mediante un proceso llamado gluconeogénesis. Esta glucosa recién formada puede ser liberada de nuevo al torrente sanguíneo para ser utilizada por otros tejidos, incluyendo los músculos, en un ciclo conocido como el ciclo de Cori. Este ciclo demuestra la eficiencia del cuerpo para reciclar y reutilizar recursos energéticos.
Además de la producción en mamíferos, la fermentación láctica también es llevada a cabo por ciertas bacterias, como las del género Lactobacillus. Estas bacterias son las responsables de la acidificación de la leche para producir yogur y queso, y también pueden encontrarse en la boca, contribuyendo al proceso de formación de caries dentales.
Desmintiendo Mitos: Ácido Láctico, Ejercicio y Dolor Muscular
Durante mucho tiempo, el ácido láctico fue injustamente culpado de la acidosis muscular y el dolor (las populares 'agujetas') experimentado después de un ejercicio intenso. Sin embargo, la ciencia moderna ha desmentido esta creencia, revelando una comprensión mucho más matizada de lo que ocurre en nuestros músculos.
En primer lugar, es fundamental entender que, a pH fisiológico (alrededor de 7.35 en el cuerpo humano), el ácido láctico no se encuentra en su forma ácida, sino disociado como lactato. El ácido láctico tiene un pKa de 3.86, lo que significa que en las condiciones del cuerpo, libera su protón y se convierte en el anión lactato. Por lo tanto, no es el "ácido láctico" el que se acumula y causa acidez directamente.
Entonces, ¿qué causa la acidosis durante el ejercicio extremo? La verdadera culpable es la hidrólisis del ATP. Cuando el ATP se descompone para liberar energía, se libera un catión hidrógeno (H+). Durante un ejercicio de alta intensidad, la producción de ATP es masiva para satisfacer la demanda muscular. La gran cantidad de ATP producido e hidrolizado en un corto período de tiempo genera una acumulación significativa de estos cationes hidrógeno, que superan la capacidad de los sistemas amortiguadores (buffers) del cuerpo para neutralizarlos. Esta acumulación de H+ es la principal responsable de la disminución del pH y la consiguiente acidosis. La producción de lactato, de hecho, ayuda a mitigar la acidosis al consumir H+ como parte de la reacción de la LDH para regenerar NAD+.

En cuanto al dolor muscular post-ejercicio (agujetas), la evidencia actual sugiere que no es causado por la acumulación de lactato. En cambio, se atribuye a microrroturas en las fibras musculares y a una respuesta inflamatoria posterior. El lactato, por el contrario, es un proceso benéfico que permite la continuidad de la producción de energía y, por ende, del ejercicio.
Aplicaciones Sorprendentes del Ácido Láctico
Más allá de su rol biológico, el ácido láctico y sus derivados encuentran una amplia gama de aplicaciones en diversas industrias, gracias a sus propiedades únicas.
En Medicina
Una de las aplicaciones médicas más conocidas es su inclusión en la solución láctica de Ringer, también conocida como solución de Hartmann. Esta solución intravenosa se utiliza para reponer líquidos y electrolitos en pacientes que han sufrido pérdida de sangre debido a traumatismos, cirugías o quemaduras. La solución de Ringer lactato está compuesta por electrolitos como sodio (Na+), cloro (Cl-) y, por supuesto, lactato (L-lactato). A diferencia de la solución salina fisiológica (0.9%), la solución de Ringer lactato tiende a tener un efecto más alcalinizante en el cuerpo debido a la metabolización del lactato en bicarbonato en el hígado, lo que ayuda a corregir la acidosis en ciertos escenarios clínicos. Es una alternativa valiosa para la recuperación de volumen y el mantenimiento del equilibrio ácido-base.
En Cosmética
El ácido láctico es un componente muy valorado en la industria cosmética, especialmente como un agente anti-edad y un suavizante de la piel. Al ser un α-hidroxílico (AHA), actúa como un exfoliante suave, ayudando a remover las células muertas de la superficie de la piel. Sus beneficios incluyen:
- Suavizar contornos: Mejora la textura general de la piel.
- Reducir el daño solar: Ayuda a minimizar la apariencia de manchas y líneas finas causadas por la exposición al sol.
- Mejorar el tono y la textura: Contribuye a una piel más uniforme y luminosa.
A menudo se utiliza como una alternativa más amplia a la glicerina como suavizante. Sin embargo, es crucial tomar precauciones al usar productos con ácido láctico, ya que pueden aumentar la sensibilidad de la piel a los rayos UV del sol, haciendo indispensable el uso de protector solar.
En la Industria Alimentaria
En el ámbito alimentario, el ácido láctico es un regulador de acidez muy común. Aunque puede derivarse de la lactosa de la leche, gran parte del ácido láctico comercial se produce mediante la fermentación de fuentes de carbohidratos como el almidón de maíz, utilizando bacterias como Bacillus acidilacti, Lactobacillus delbrueckii o L. bulgaricus. Esto es importante para los consumidores vegetarianos o veganos, ya que lo que comúnmente se denomina “leche ácida” en las etiquetas de los alimentos no siempre implica un origen lácteo directo, sino que puede referirse al ácido láctico como ingrediente.
Otras Aplicaciones
La versatilidad del ácido láctico se extiende a otros campos:
- Alimento para niños: En ciertas formulaciones.
- Purgante: En la forma de lactato de calcio o lactato de magnesio.
- Removedor de sales de calcio: Utilizado en procesos industriales.
- Mordiente: En la industria textil para fijar tintes.
- Curtimiento de pieles: Contribuye al procesamiento del cuero.
- Materia prima para síntesis orgánica: Su grupo hidroxilo y carboxilo lo hacen un bloque de construcción valioso para la creación de otras moléculas orgánicas.
- Acción acaricida: Se emplea en el control de la varroasis, una enfermedad causada por el ácaro Varroa destructor que afecta a las abejas melíferas (Apis mellifera), demostrando su utilidad incluso en la apicultura.
El descubrimiento del ácido láctico por el químico sueco Carl Wilhelm Scheele, uno de los primeros ácidos conocidos, marcó un hito en la química. Desde entonces, su estudio ha revelado una molécula con una importancia que abarca desde la bioquímica esencial de la vida hasta innovadoras aplicaciones industriales y médicas.
Preguntas Frecuentes sobre el Ácido Láctico y su Nitrilo
¿Qué diferencia hay entre el ácido láctico y el lactato?
El ácido láctico es la forma molecular completa (H3C-CH(OH)-COOH). El lactato es el anión que se forma cuando el ácido láctico pierde un protón (H+) en una solución, especialmente a pH fisiológico. En el cuerpo humano, el 99% del ácido láctico se encuentra en su forma disociada, es decir, como lactato, debido al pH de la sangre y los tejidos.
¿Es el ácido láctico el causante de las agujetas o el dolor muscular?
No, esta es una creencia popular incorrecta. La evidencia científica actual indica que las agujetas (dolor muscular de aparición tardía) son causadas por microrroturas en las fibras musculares y la respuesta inflamatoria posterior, no por la acumulación de lactato. De hecho, la producción de lactato es un proceso beneficioso que ayuda a mantener la producción de energía durante el ejercicio intenso.
Si el lactato no causa acidosis, ¿qué la provoca durante el ejercicio intenso?
La acidosis durante el ejercicio intenso es principalmente causada por la hidrólisis del ATP (adenosín trifosfato), la molécula de energía del cuerpo. Cuando el ATP se descompone para liberar energía, también libera cationes de hidrógeno (H+). Durante el ejercicio de alta intensidad, se hidroliza una gran cantidad de ATP, lo que produce una acumulación de H+ que supera la capacidad de los sistemas amortiguadores del cuerpo, llevando a una disminución del pH y, por ende, a la acidosis.
¿Cómo se produce el L-lactato en el cuerpo?
El L-lactato se produce a partir del piruvato mediante la acción de la enzima lactato deshidrogenasa (LDH). Esta reacción es crucial porque regenera el NAD+ (nicotinamida adenina dinucleótido) a partir del NADH + H+. El NAD+ es esencial para que la glucólisis, la vía principal de producción de ATP en ausencia de suficiente oxígeno, pueda continuar y así asegurar el suministro de energía a los músculos durante el esfuerzo intenso.
¿Cuál es la función del ciclo de Cori?
El ciclo de Cori describe la ruta metabólica en la que el lactato producido en los músculos durante el ejercicio es transportado al hígado. En el hígado, el lactato se convierte de nuevo en glucosa mediante la gluconeogénesis. Esta glucosa puede ser liberada al torrente sanguíneo para ser utilizada por los músculos u otros tejidos, completando un ciclo de reciclaje de energía entre el músculo y el hígado.
¿Se utiliza el ácido láctico en cosméticos? ¿Es seguro?
Sí, el ácido láctico se utiliza ampliamente en cosméticos como un alfa-hidroxiácido (AHA) para exfoliar la piel, mejorar su textura y tono, y reducir los signos del envejecimiento. Generalmente es seguro cuando se usa según las indicaciones, pero es crucial tener en cuenta que puede aumentar la sensibilidad de la piel a los rayos UV del sol. Por lo tanto, el uso de protector solar es indispensable al usar productos que contengan ácido láctico.
¿Se puede encontrar ácido láctico en alimentos que no sean lácteos?
Sí. Aunque su nombre proviene de la leche, la mayoría del ácido láctico utilizado comercialmente en alimentos se produce por fermentación bacteriana de carbohidratos no lácteos, como el almidón de maíz. Por lo tanto, muchos alimentos etiquetados como "vegetarianos" o "veganos" pueden contener ácido láctico como regulador de acidez sin que provenga de productos lácteos directamente.
Si quieres conocer otros artículos parecidos a El Nitrilo del Ácido Láctico: Formación y Usos puedes visitar la categoría Librerías.
