23/05/2023
En el vasto universo de la termodinámica, comprender por qué ciertos procesos ocurren de forma natural mientras que otros no, es fundamental. Tradicionalmente, la Segunda Ley de la Termodinámica nos enseña que un proceso es espontáneo si la entropía total del universo (sistema + entorno) aumenta. Sin embargo, calcular los cambios de entropía del entorno puede ser un desafío. Aquí es donde entra en juego un concepto más práctico y central para la química: la energía libre de Gibbs. Esta función de estado nos permite predecir la dirección de una reacción química y la composición de un sistema en equilibrio, centrándonos exclusivamente en las propiedades del sistema bajo condiciones de temperatura y presión constantes, que son las más comunes en los laboratorios y en la naturaleza.

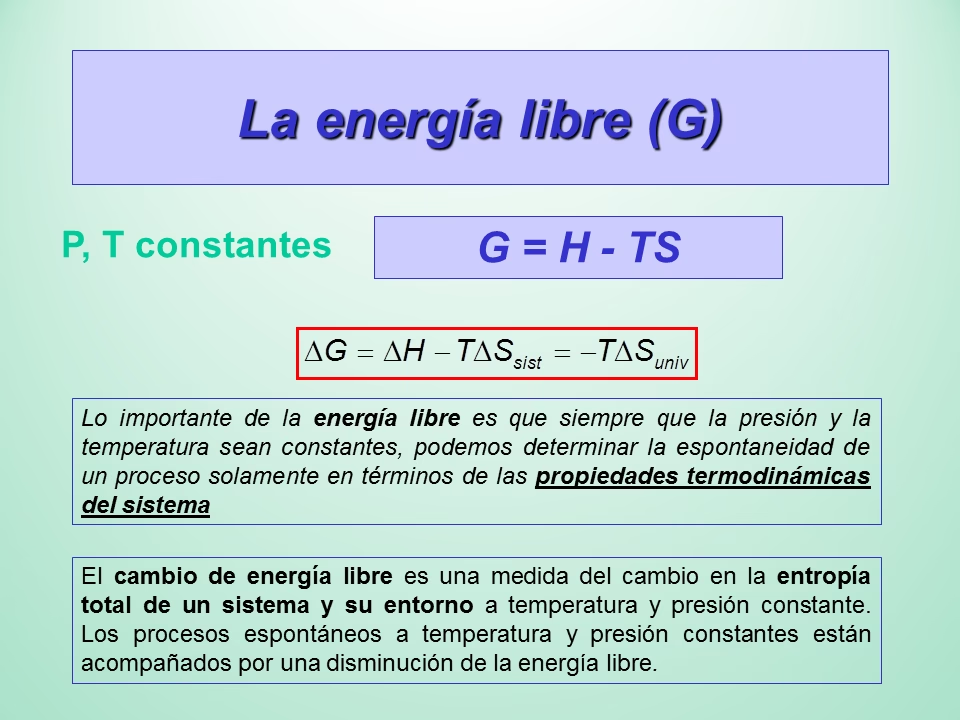
La energía libre de Gibbs, a menudo simplemente referida como energía de Gibbs o potencial de Gibbs, es una función termodinámica definida por la ecuación fundamental:
G = H – TS
Donde G es la energía de Gibbs, H es la entalpía del sistema, T es la temperatura absoluta y S es la entropía del sistema. Dado que H, T y S son todas funciones de estado, G también lo es. Esto significa que el cambio en la energía de Gibbs (ΔG) para cualquier proceso solo depende de los estados inicial y final del sistema, no del camino que se tome. Para un cambio de estado a temperatura constante, podemos expresar esta relación de manera crucial:
ΔG = ΔH – TΔS
- La Conexión Esencial con la Entropía Total del Mundo
- Energía de Gibbs y el Cambio Químico: La Variable Maestra
- La Influencia Crucial de la Temperatura en la Espontaneidad
- Energía de Gibbs Estándar (ΔG°): Un Punto de Referencia
- ΔG vs. ΔG°: Una Distinción Crucial
- Interpretación de los Cambios de Energía de Gibbs Estándar
- Encontrando la Temperatura de Equilibrio
- Preguntas Frecuentes sobre la Energía Libre
La Conexión Esencial con la Entropía Total del Mundo
La simplicidad de la ecuación ΔG = ΔH – TΔS puede hacer que uno se pregunte cómo engloba el cambio de entropía total del mundo (ΔS_total), que es, en última instancia, el verdadero criterio para la espontaneidad. La clave reside en cómo el sistema interactúa con su entorno. La mayoría de las reacciones químicas son exotérmicas o endotérmicas, lo que implica un flujo de calor (q_p) entre el sistema y el entorno a presión constante. El cambio de entalpía (ΔH) de una reacción se define como el calor absorbido por el sistema del entorno. Por lo tanto, el calor liberado al entorno es -q_p, lo que provoca un cambio en la entropía del entorno de ΔS_entorno = -q_p / T = -ΔH / T.
Si recordamos la Segunda Ley de la Termodinámica, ΔS_total = ΔS_entorno + ΔS_sistema. Sustituyendo ΔS_entorno, obtenemos:
ΔS_total = (-ΔH / T) + ΔS_sistema
Multiplicando ambos lados por -T, llegamos a:
-TΔS_total = ΔH - TΔS_sistema
Al comparar esta ecuación con la definición de ΔG, podemos ver claramente que ΔG = -TΔS_total. Esto nos lleva a la conclusión fundamental: si ΔS_total es positivo (indicando un proceso espontáneo), entonces ΔG debe ser negativo (ya que T es siempre positivo en Kelvin). Por lo tanto, un proceso que ocurre a temperatura y presión constantes será espontáneo si y solo si ΔG disminuye. Este es el criterio más útil y práctico para predecir la dirección de las reacciones químicas.
Energía de Gibbs vs. Energía de Helmholtz: Una Breve Distinción
Aunque en este artículo nos centraremos principalmente en la energía de Gibbs, es importante mencionar que existe otra función de energía libre conocida como energía de Helmholtz (A = U – TS). La energía de Helmholtz es el criterio de espontaneidad para procesos que ocurren a temperatura y volumen constantes. Mientras que la energía de Gibbs es de mayor interés para los químicos (dado que la mayoría de las reacciones se realizan a presión constante, como en un vaso de precipitados abierto a la atmósfera), la energía de Helmholtz es relevante en campos como la ingeniería química, donde los procesos a menudo se confinan a reactores de volumen fijo.
Energía de Gibbs y el Cambio Químico: La Variable Maestra
La importancia de la función de Gibbs en la química es inmensa. Sirve como la única variable maestra que determina si un cambio químico dado es termodinámicamente posible y, si lo es, en qué dirección y hasta qué punto procederá. Las condiciones de temperatura y presión constantes son cruciales para la validez de ΔG como criterio de espontaneidad.
ΔG < 0: La reacción puede proceder espontáneamente hacia adelante (productos). Por ejemplo,A → B.ΔG > 0: La reacción no es espontánea hacia adelante; en cambio, la reacción inversa es espontánea. Por ejemplo,A ← B.ΔG = 0: La reacción se encuentra en equilibrio. En este punto, no hay cambio neto en las concentraciones de reactivos y productos. Por ejemplo,A ⇌ B.
Un ejemplo clásico es la congelación del agua: H₂O(l) → H₂O(s). Por debajo de su punto de congelación, el agua líquida experimenta una disminución en su entropía al solidificarse, pero el calor liberado al entorno lo compensa con creces, aumentando la entropía total del mundo y, por lo tanto, disminuyendo la energía libre del agua. Esto impulsa el proceso espontáneamente.
Una consecuencia vital de la tendencia unidireccional de la energía libre a disminuir es que, una vez que alcanza su valor mínimo posible, todo cambio neto se detiene. Este es el estado de equilibrio químico.
La Influencia Crucial de la Temperatura en la Espontaneidad
La ecuación ΔG = ΔH – TΔS revela que la dependencia de la temperatura de ΔG depende significativamente del signo de ΔH (cambio de entalpía) y ΔS (cambio de entropía). Aunque los valores de ΔH y ΔS también varían ligeramente con la temperatura, su signo es el factor dominante. Esto da lugar a cuatro casos posibles para la espontaneidad de una reacción con respecto a la temperatura:
| Caso | Signo de ΔH | Signo de ΔS | Efecto de la Temperatura en ΔG | Espontaneidad |
|---|---|---|---|---|
| 1 | Negativo (Exotérmica) | Positivo (Aumento de desorden) | ΔG siempre negativo | Espontánea a todas las temperaturas |
| 2 | Negativo (Exotérmica) | Negativo (Disminución de desorden) | ΔG negativo solo a bajas T | Espontánea a bajas temperaturas |
| 3 | Positivo (Endotérmica) | Positivo (Aumento de desorden) | ΔG negativo solo a altas T | Espontánea a altas temperaturas |
| 4 | Positivo (Endotérmica) | Negativo (Disminución de desorden) | ΔG siempre positivo | Nunca espontánea a ninguna temperatura |
Es fundamental comprender estas relaciones en lugar de memorizarlas. La posición de la línea ΔH en relación con la línea TΔS, y la pendiente de esta última (determinada por el signo de ΔS), son las características diferenciadoras clave.
Energía de Gibbs Estándar (ΔG°): Un Punto de Referencia
Al igual que con la entalpía (ΔH°) y la energía interna (ΔU°), existe el concepto de la energía de Gibbs estándar (ΔG°), donde el superíndice ° indica que todos los componentes (reactivos y productos) se encuentran en sus estados estándar. Las definiciones convencionales de los estados estándar son:
- Gases: Presión parcial de 1 atmósfera.
- Líquidos puros: El líquido bajo una presión total de 1 atm.
- Solutos: Una concentración efectiva de 1 mol L⁻¹ (aproximadamente 10⁻⁴ molar o menos para concentraciones reales).
- Sólidos: El sólido puro bajo una presión de 1 atm.
Aunque no existe una 'temperatura estándar' explícita, la mayoría de las tablas termodinámicas listan valores a 298.15 K (25°C), por lo que esta temperatura suele estar implícita. Es crucial no confundir estos estados estándar termodinámicos con las condiciones de 'Temperatura y Presión Estándar' (STP) utilizadas en los cálculos de la ley de los gases.
Para predecir los cambios químicos, necesitamos conocer las energías libres de los componentes individuales de la reacción. La energía libre de formación estándar (ΔG°f) de una sustancia se puede calcular combinando su entalpía de formación estándar (ΔH°f) y su entropía estándar (S°):
ΔG°f = ΔH°f – TΔS°f
El ΔG°f de una sustancia representa el cambio de energía libre asociado a la formación de la sustancia a partir de sus elementos en sus formas más estables bajo condiciones estándar (1 atm, 298 K). Para los elementos en sus estados estándar, ΔG°f es, por definición, cero. Los iones en solución acuosa son un caso especial; sus energías libres estándar son relativas al ion hidrógeno hidratado (H⁺(aq)), al que se le asigna ΔG°f = 0.
Una vez que se conocen los valores de ΔG°f para todos los reactivos y productos, el cambio de energía de Gibbs estándar para la reacción (ΔG°) se calcula de manera análoga a ΔH°:
ΔG° = ΣΔG°f (productos) – ΣΔG°f (reactivos)
Ejemplo de Cálculo de ΔG°
Consideremos la descomposición del carbonato de calcio:
CaCO₃(s) → CaO(s) + CO₂(g)
Los valores de ΔG°f son: CaCO₃(s): -1128 kJ/mol, CaO(s): -603.5 kJ/mol, CO₂(g): -137.2 kJ/mol.
ΔG° = (-603.5 - 137.2) - (-1128) kJ/mol = +130.9 kJ/mol
Este valor positivo de ΔG° indica que el proceso no es espontáneo en condiciones estándar a 25°C (es decir, el carbonato de calcio sólido no se descompondrá en óxido de calcio sólido y CO₂ a una presión parcial de 1 atm). Sin embargo, esta reacción se lleva a cabo a gran escala en la industria para fabricar cemento, lo que demuestra que puede ser espontánea bajo diferentes condiciones (generalmente a temperaturas elevadas).
ΔG vs. ΔG°: Una Distinción Crucial
Es vital entender la diferencia entre ΔG y ΔG°. Mientras que ΔG° se refiere a un cambio químico bajo condiciones únicas y específicas (estados estándar), el valor de ΔG varía continuamente a medida que una reacción progresa y las concentraciones de reactivos y productos cambian. Para una reacción dada, hay un número infinito de valores de ΔG posibles, dependiendo de la composición de la mezcla de reacción en un momento dado.
El punto de equilibrio de una reacción corresponde al mínimo de la energía de Gibbs (ΔG = 0). Si la reacción comienza con una composición donde ΔG es negativo, procederá espontáneamente hacia adelante hasta alcanzar el equilibrio. Si comienza con una composición donde ΔG es positivo, procederá espontáneamente hacia atrás hasta el equilibrio. La razón de este mínimo de energía de Gibbs en el equilibrio está relacionada con el aumento de la entropía cuando los productos y reactivos coexisten en la misma fase; incluso una mínima "contaminación" de los productos puros por los reactivos reduce la energía libre.
Un ΔG° negativo no significa que los reactivos se transformarán completamente en productos; significa que en el equilibrio, habrá más productos que reactivos bajo condiciones estándar. De manera similar, un ΔG° positivo no significa que no se formen productos en absoluto; significa que en el equilibrio, habrá más reactivos que productos.
Interpretación de los Cambios de Energía de Gibbs Estándar
Aunque ΔG es el criterio real de espontaneidad, los valores de ΔG° son muy útiles para obtener una idea general de la viabilidad de una reacción:
- Reacciones con
ΔG°muy negativo: Suelen ser espontáneas y prácticamente completas bajo casi cualquier condición razonable. Por ejemplo, la combustión o la formación de moléculas estables como el agua (ΔG° = -237.2 kJpara la formación deH₂O(l)), que es termodinámicamente muy estable. - Reacciones con
ΔG°muy positivo: Indican que la reacción directa es muy improbable en condiciones estándar. Por ejemplo, la disociación de una molécula estable en sus átomos (ΔG° = +406.6 kJparaH₂O(g) → 2 H(g) + O(g)). - Reacciones con
ΔG°cercano a cero: Son altamente sensibles a cambios en temperatura y presión, y la composición en el equilibrio puede contener cantidades significativas de reactivos y productos. Un ejemplo es la disociación del tetróxido de dinitrógeno:N₂O₄(g) → 2 NO₂(g)conΔG° = +2.8 kJ. Este pequeño valor positivo implica que la reacción es sensible a las condiciones y puede desplazarse fácilmente. - Reacciones en solución acuosa (iones): Se debe ser cuidadoso. Aunque el
ΔG°para la disociación del agua (H₂O(l) → H⁺(aq) + OH⁻(aq)) es+79.9 kJ, lo que predice que el agua no formará concentraciones 1M de iones, sabemos por el producto iónico del agua (Kw = 10⁻¹⁴) que una pequeña pero constante disociación ocurre. - Cambios de fase: Para la vaporización del agua (
H₂O(l) → H₂O(g)),ΔG° = 8.58 kJa 25°C. Esto significa que a 25°C y 1 atm de presión parcial de vapor de agua, la conversión no es espontánea. El agua líquida a 25°C solo se evaporará espontáneamente si la presión parcial del vapor de agua en el aire es inferior a su presión de vapor de equilibrio (0.031 atm a 25°C).
Encontrando la Temperatura de Equilibrio
Cuando una reacción está en equilibrio, ΔG = 0. Si aproximamos ΔH y ΔS por sus valores estándar (ΔH° y ΔS°), podemos estimar la temperatura a la que una reacción alcanza el equilibrio:
0 = ΔH° – TΔS°
Por lo tanto:
T = ΔH° / ΔS°
¡Precaución importante! Un error muy común es olvidar que ΔH° se expresa normalmente en kilojulios (kJ) y ΔS° en julios (J), por lo que es esencial convertir ambas unidades para que sean consistentes (ej. ambas en julios).
Por ejemplo, para estimar el punto de ebullición normal del agua (H₂O(l) → H₂O(g)), si ΔH° = 44.1 kJ/mol (44100 J/mol) y ΔS° = 118.7 J/mol·K:
T = 44100 J/mol / 118.7 J/mol·K ≈ 371.5 K
Este valor (371.5 K o 98.35°C) está muy cerca del punto de ebullición real del agua (373 K o 100°C). La pequeña diferencia se debe a que ΔH° y ΔS° tienen una ligera dependencia de la temperatura y estamos utilizando valores estándar a 25°C. Sin embargo, la capacidad de estimar el punto de ebullición de un líquido a partir de datos termodinámicos es impresionante.
Preguntas Frecuentes sobre la Energía Libre
¿La energía libre es realmente "libre"?
El término "energía libre" puede ser engañoso. No significa que la energía se obtenga sin costo o que sea ilimitada. Se refiere a la máxima cantidad de trabajo no-PV (no relacionado con la expansión o contracción) que un sistema puede realizar a temperatura y presión constantes. Es la porción de la energía total del sistema que está "disponible" para hacer trabajo útil.
¿Qué significa que una reacción sea espontánea?
En termodinámica, espontáneo significa que una reacción tiene una tendencia inherente a ocurrir sin la necesidad de una intervención externa continua (como añadir energía). Sin embargo, la espontaneidad termodinámica no nos dice nada sobre la velocidad a la que ocurrirá la reacción (cinética). Una reacción puede ser termodinámicamente espontánea (ΔG < 0) pero proceder tan lentamente que, en la práctica, no se observe ningún cambio.
¿Siempre se produce una reacción si ΔG es negativo?
Sí, termodinámicamente, una reacción con un ΔG negativo tiene la tendencia a producirse. Sin embargo, como se mencionó, si la barrera de activación para la reacción es muy alta, la velocidad de reacción puede ser insignificante. Por ejemplo, la oxidación del diamante a grafito es termodinámicamente espontánea a temperatura ambiente, pero no la observamos porque la velocidad de reacción es extremadamente lenta.
¿Cómo se relaciona la energía de Gibbs con la constante de equilibrio?
La energía de Gibbs está estrechamente ligada a la constante de equilibrio (K) de una reacción. Para una reacción en equilibrio, ΔG = 0. La relación entre ΔG° y K es ΔG° = -RT ln K. Esta ecuación muestra que un ΔG° negativo implica una constante de equilibrio grande (favoreciendo los productos), mientras que un ΔG° positivo implica una constante de equilibrio pequeña (favoreciendo los reactivos).
En resumen, la energía libre de Gibbs es una herramienta poderosa e indispensable en química y otras ciencias para entender la dirección y el alcance de los procesos. Al considerar la entalpía y la entropía dentro de un solo parámetro, nos permite predecir la espontaneidad y el equilibrio de las reacciones de una manera elegante y práctica, revelando la "fuerza motriz" detrás de los cambios en el mundo que nos rodea.
Si quieres conocer otros artículos parecidos a La Energía Libre de Gibbs: Clave de la Espontaneidad puedes visitar la categoría Librerías.